
EEGفعالیت الکتریکی مغز را از طریق الکترودهایی که روی پوست سر قرار میگیرند، ثبت میکند. در گزارشهای QEEG، پزشکان معمولاً تلاش میکنند بفهمند که کدام ناحیه از سر بیشترین قدرت را در یک باند فرکانسی خاص دارد تا محل احتمالی ناهنجاری را تشخیص دهند.
دو رویکرد کلی برای این کار وجود دارد:
Source-based localization که از طریق مدل سازی معکوس تلاش میکند منبع درون مغزی سیگنال را تخمین بزند.
Sensor-based localization که به طور مستقیم فعالیت را در سطح الکترودها (یعنی همانجایی که سیگنال ثبت شده) بررسی میکند.
در عمل، در بیشتر استفادههای بالینی روزمره QEEG، از روش دوم یعنی sensor-level localization استفاده میشود؛ چرا که این روش مستقیمتر، قابل فهمتر و بر پایه نوروفیزیولوژی شناخته شده است. در این مقاله، ابتدا تئوری پشت هر روش را بررسی میکنیم و سپس توضیح میدهیم که چرا روش مبتنی بر sensor برای پزشکان مفیدتر است. بعد، نُرمهای شناخته شده مربوط به توزیع فرکانس ناحیه (مثلاً آلفا در occipital، یا بتا در frontal) را معرفی کرده و میگوییم که انحراف از این الگوها چه معانی بالینی میتواند داشته باشد. در نهایت، به ارتباط بین الگوهای توپوگرافیک sensor-level با اختلالاتی مانند ADHD، افسردگی، اضطراب، و اختلال شناختی میپردازیم، همراه با مثالهای بالینی.
Source localization سعی دارد (مسئله معکوس EEG) را حل کند؛ یعنی با توجه به سیگنال ثبت شده در پوست سر، تخمین بزند که منبع درون مغز (مثلاً در قشر مغزی) که این فعالیت را ایجاد کرده کجاست. روشهایی مانند LORETA یا sLORETA از مدلهای بیو فیزیکی سر استفاده میکنند تا محل منبع را در فضای سه بعدی مغز تخمین بزنند.
با اینکه در تئوری میتوان حتی نواحی عمیق قشر مغز را تعیین کرد، در عمل این مسئله ill-posed است؛ یعنی با دادههای محدود (مثلاً از ۱۹ تا ۲۱ الکترود که در QEEGهای معمولی استفاده میشود) بینهایت پیکر بندی ممکن برای منبع وجود دارد که همه میتوانند داده را توجیه کنند. به عبارت دیگر، اطلاعات کافی برای تعیین دقیق منبع وجود ندارد.
به علاوه، کوچکترین خطا در مدل سازی یا وجود آرتیفکت میتواند منجر به مکان یابی نادرست شود. برای مثال، فعالیت عضلات گردن ممکن است به اشتباه به ناحیهی occipital مغز نسبت داده شود. همچنین، محاسبهی z-scoreهای نرمال در این روشها نیاز به فرضیاتی دربارهی هدایت الکتریکی سر، محل دقیق الکترودها، و ساختار مغز دارد؛ اگر این فرضیات دقیق نباشند، نتایج گمراه کننده میشوند.
در مقابل، sensor-based localization بر پایه دادهی واقعی ثبت شده در سطح پوست سر عمل میکند. در این روش، هیچ مدل سازی معکوس یا الگوریتمی روی دادهها اعمال نمیشود. به سادگی بررسی میشود که در هر باند فرکانسی، قدرت سیگنال در کدام الکترود بیشتر است. بهعبارت دیگر، سؤال این است که: روی سر، این ریتم کجا بیشترین قدرت را دارد؟
این روش با فیزیولوژی مغز هم راستاست. برای مثال، آلفای مرتبط با آرامش معمولاً از قشر occipital نشأت میگیرد، بنابراین در افراد نرمال، این ریتم در الکترودهای occipital قویتر است. اگر نقشهی توپوگرافیک یک بیمار نشان دهد که آلفا در frontal قویتر است، این موضوع بلافاصله به عنوان انحراف از الگوی نرمال شناخته میشود.
مطالعات نشان دادهاند که برای داشتن تصویر برداری دقیق از منابع درون مغزی، نیاز به چیدمان با تراکم بالا (یعنی بیش از ۶۴ کانال) داریم. اما در QEEG های بالینی معمول، اغلب از ۱۹ تا ۲۱ کانال استفاده میشود، که دقت فضایی لازم را ندارد و سیگنالهای متمرکز ممکن است به صورت مناطق گسترده و نامشخص دیده شوند. همچنین، در تصاویر source، تشخیص آرتیفکتها دشوارتر است. برای مثال، نویز عضلانی یا حرکت چشم که در نقشه پوست سر به وضوح در الکترودهای خاص دیده میشود، ممکن است در تصویر source به اشتباه به مغز نسبت داده شود.
برخلاف این، نقشههای sensor-based نشان میدهند که واقعاً چه چیزی در الکترودها ثبت شده است، و مکان یابی نادرست را کاهش میدهند.
قابلیت تفسیر مستقیم: پزشکان آموزش دیدهاند که EEG را براساس الگوهای سطح سر تفسیر کنند. اگر نقشه نشان دهد که بتا در ناحیه frontal بیشتر است، بلافاصله توجه به frontal جلب میشود. اما تصویر سه بعدی از مغز که همین داده را نشان میدهد، ممکن است نیاز به دانش پیشرفته داشته باشد.
قابلیت بیان ساده: یافتهها را میتوان به زبان ساده بیان کرد، مثلاً: «موجهای سریع شما در frontal قویتر هستند»، بدون نیاز به معادلات پیچیده.
هم راستایی با فیزیولوژی شناخته شده: الگوهای sensor با الگوهای نرمال EEG مقایسه میشوند و هرگونه انحراف بلافاصله قابل تشخیص است.
تفسیر مستقیم: نقشههای sensor به طور دقیق نشان میدهند که کدام الکترود در هر باند فرکانسی (مثل alpha، beta) بیشترین قدرت را دارد. بیشتر پزشکان میتوانند به راحتی نواحی مختلف پوست سر (frontal، central، parietal، occipital) را با لوبهای زیرین مغز تطبیق دهند. برای مثال، اگر alpha در O1/O2 بیشترین قدرت را داشته باشد، این نشان میدهد که منشأ آن ناحیه occipital است. چون این روش دادهها را به حداقل ممکن پردازش میکند، پزشک میتواند به سادگی به بیمار توضیح دهد: «امواج سریع مغزت در frontal قویتر هستند» بدون نیاز به ریاضیات پیچیده.
هم راستایی با فیزیولوژی: الگوهای sensor با الگوهای نرمال EEG که به خوبی مستند شدهاند مقایسه میشوند. هر گونه انحراف بلافاصله به چشم میآید. مثلاً در یک فرد بالغ، انتظار داریم alpha در ناحیه occipital قویتر باشد. اگر این قدرت به frontal منتقل شده باشد، به وضوح غیر طبیعی است. همینطور، beta معمولاً در نواحی frontal و central دیده میشود؛ اگر "hotspot" آن جای دیگری باشد، غیر عادی است. در مقابل، تصاویر source اغلب با برچسب گذاری بر روی gyri مغزی همراه هستند که برای پزشکان به اندازه نقشههای پوست سر آشنا نیستند.
کاهش مکان یابی نادرست: چون نقشههای sensor از مدل سازی معکوس استفاده نمیکنند، آرتیفکتها همان جایی که واقعاً رخ دادهاند باقی میمانند. مثلاً اگر بیمار عضلات گردنش را منقبض کند، نویز با فرکانس بالا در الکترودهای temporal یا occipital دیده میشود و یک پزشک با تجربه آن را به عنوان آرتیفکت عضلانی تشخیص میدهد. اما در مدلهای source، این آرتیفکت ممکن است به اشتباه به مغز نسبت داده شود. به عبارت دیگر، sensor-based analysis واقعاً نشان میدهد که EEG چه چیزی را ثبت کرده است و این برای درک دقیق و بالینی ضروری است.
تطابق با شهود بالینی و قابلیت اقدام: یافتههای sensor-based مستقیماً با شیوهی فکر بالینی تطابق دارند. مثلاً اگر نقشهی topographic نشان دهد که alpha به طور غیر عادی در نواحی frontal بالاست، پزشک بلافاصله به تشخیصهایی مثل افسردگی، خواب آلودگی، یا اثر دارو فکر میکند. سپس ارزیابیهای خاص مانند بررسی خلق، مرور داروها یا مداخلاتی مانند neurofeedback هدفمند دنبال میشود. همچنین اگر beta در ناحیه temporal به شدت فعال باشد، احتمال اختلالات اضطرابی یا برانگیختگی بالا مطرح میشود. چون مکان هر باند فرکانسی با یافتههای بالینی خاصی مرتبط است، نقشههای sensor پزشک را مستقیماً به گامهای بعدی هدایت میکنند. در عمل، بسیاری از پزشکان ابتدا از نقشههای sensor استفاده میکنند و تحلیلهای پیچیدهتر source را فقط به عنوان ابزار تکمیلی به کار میگیرند.
وقتی نقشههای sensor ریتمهایی را نشان میدهند که در محل غیر طبیعی ظاهر شدهاند، یا الگوهای anterior/posterior غیر عادی دارند، اغلب با شرایط خاصی مرتبط هستند. در ادامه، مثالهایی برای alpha و beta آورده شده است.
در فرد بالغ بیدار، انتظار داریم که قدرت alpha در الکترودهای ناحیه occipital بیشتر باشد. اگر alpha در نواحی frontal غالب باشد، نشانهی هشدار است. یکی از یافتههای کلاسیک در افسردگی دیده میشود. بسیاری از بیماران افسرده افزایش alpha در نواحی frontal دارند اغلب در سمت چپ بیشتر از راست است. این ناقرینگی آلفا در نواحی frontal نشانهی کاهش فعالیت frontal idling است و با علائمی مانند بی انگیزگی مرتبط است. در نقشه sensor، اگر «hotspot» آلفا به جای O1/O2 در F3/F7 باشد، بررسی برای اختلالات خلقی ضروری میشود.
دلایل دیگری هم برای frontal alpha وجود دارد. مثلاً کاهش شناختی یا آسیب مغزی میتواند باعث شود نواحی posterior نتوانند آلفای نرمال تولید کنند، و در عوض ریتمهای کندتر در نواحی frontal پدیدار شوند. مطالعات نشان دادهاند که بیماران با اختلال شناختی خفیف یا آسیب منتشر قشری، آلفای occipital ضعیف و در عوض آلفای frontal قویتری دارند. داروها نیز نقش دارند؛ مثلاً benzodiazepine ها و سایر آرام بخشها میتوانند باعث افزایش گستردهی alpha یا beta شده و توزیع آن را به جلو منتقل کنند.
در مجموع، آلفای غالب در ناحیه posterior نرمال است. اگر قلهی آلفا به frontal منتقل شود، باید احتمال افسردگی، مصرف داروهای آرام بخش یا اختلالات قشری را در نظر گرفت.
Beta با دامنهی کم، معمولاً در نواحی frontal/central در بیداری دیده میشود. اگر beta به طور غیر عادی در نواحیposterior (occipital/parietal) قوی باشد، معمولاً نشان دهنده برانگیختگی بیش از حد CNS hyperarousal است. یک الگوی شناخته شده در اضطراب و حملات پانیک دیده میشود. در QEEG، افراد مضطرب اغلب «hot temporals» دارند، یعنی قدرت beta در T3/T4 بالا میرود. در یک مطالعه بزرگ، علائم اضطرابی (ترس، وحشت و...) با beta > 17%و high-beta > 10% در T3/T4 ارتباط قوی داشتند. بنابراین، hotspot های beta در نواحی temporal یا occipital در نقشه sensor ممکن است نشان دهنده اضطراب یا اختلالات برانگیختگی باشند.
در مقابل، الگوی نرمال beta در ناحیهی sensorimotor (مثلاً قلهای در Cz یا Fz) طبیعی است. افزایش beta در ناحیه frontal میتواند به دلیل تمرکز یا اضطراب باشد. جالب اینجاست که برخی زیر گروههای ADHD دارای افزایش فعالیت beta هستند. تحقیقات نشان دادهاند که زیر گروهی از مبتلایان به ADHD با نام overaroused ADHDدارای beta و fast alpha بالا هستند و علائم شدیدتری هم دارند. بنابراین، وجود beta بالا در بیماری با علائم مشابه ADHD میتواند نشان دهنده این زیر گروه یا اضطراب هم زمان باشد.
همانندalpha ، اثر دارو و سطح هوشیاری اهمیت دارد. benzodiazepineها به طور مشخص beta را زیاد میکنند، حتی در نواحی posterior، و خواب آلودگی ساده هم ممکن است باعث alpha/beta posterior شود. بنابراین، هر beta غیر منتظرهای باید در بستر بالینی تفسیر شود: سطح اضطراب بررسی شود، اثر داروها لحاظ شود، و آرتیفکت عضلانی رد شود.
در عمل، پزشک نقشهی هر فرکانس را مانند نقشهای جغرافیایی نگاه میکند و از خود میپرسد:
آیا قلهی alpha همانطور که انتظار داریم در عقب است؟ آیا beta در جلوست؟ آیا موجهای کند در جای درست هستند؟
اگر نقشه با این الگوهای طبیعی مغایرت داشته باشد، مشخص میشود که باید در کجا به دنبال مشکل گشت.
مردی ۳۰ ساله با شکایت از حواس پرتی مراجعه میکند. نقشهی QEEG او تتای متوسط در Cz و همچنین hotspot beta در الکترود T4 (temporal راست) نشان میدهد. به جای نسبت دادن همه علائم بهADHD ، پزشک متوجه تمرکز بتا در temporal راست شده و به اضطراب مشکوک میشود. غربالگری انجام شده اختلال اضطراب فراگیر (GAD) را تأیید میکند. درمان اضطراب (رواندرمانی، تغییر سبک زندگی) آغاز شده و در کنار درمان توجه ادامه مییابد.
زنی ۵۰ ساله از کاهش انرژی شکایت دارد. QEEG افزایش غیر معمول آلفا در نواحی frontal چپ (F3) و ضعف آلفای posterior را نشان میدهد. با وجودی که بیمار میگوید «غمگین نیستم»، اما ناقرینگی آلفای frontal نگران کننده است. بررسی دقیقتر، علائم خفیف افسردگی را آشکار میکند. درمان (روان درمانی، احتمالاً SSRI) آغاز میشود و علائم بهبود مییابد.
مردی ۶۸ ساله با شکایت از مشکلات حافظه مراجعه میکند. QEEG او کاهش قابل توجه آلفا در occipital و افزایش تتای منتشر را نشان میدهد. فرکانس قلهی آلفا ۸.۸ هرتز است (که پایینتر از حد نرمال ۱۰ هرتز است). این یافتهها نشاندهنده کندی قشری بوده و باعث انجام تستهای نوروشناختی میشود. اختلال شناختی خفیف (MCI) تشخیص داده شده و درمان توانبخشی شناختی آغاز میشود.
کاهش مکان یابی اشتباه: چون دادهها مستقیماً از سطح الکترودها استفاده میشوند، آرتیفکتها به جای اینکه به مغز نسبت داده شوند، در محل واقعیشان باقی میمانند.
ارتباط بالینی قوی: توپوگرافیهای sensor مستقیماً با تفکر و تصمیم گیری بالینی مرتبط هستند. مثلاً، آلفای غیر طبیعی در frontal ممکن است نشان دهنده افسردگی، خواب آلودگی یا مصرف داروهای آرام بخش باشد.
آلفا (۸ تا ۱۲ هرتز): این ریتم در بزرگسالان بیدار، آرام و چشم بسته غالب است. منبع آن ناحیهی occipital است، بنابراین آلفا در ناحیهی posterior بیشترین قدرت را دارد. باز شدن چشم یا توجه باعث کاهش آلفا میشود.
بتا (۱۳ تا ۳۰ هرتز): دامنهای کمتر از آلفا دارد و در نواحی frontal و central بیشتر دیده میشود. با فعالیت ذهنی و هوشیاری مرتبط است. بتای منتشر و قوی ممکن است نشانه مصرف داروهای آرام بخش مانند benzodiazepine باشد. در حالت استراحت، بتا در نواحی posterior معمولاً ضعیف است.
تتا (۴ تا ۷ هرتز): در خواب آلودگی، برخی فعالیتهای شناختی، و در کودکان شایع است. تتای مرکزی زیاد میتواند نشاندهنده ADHD یا افت شناختی باشد، ولی به تنهایی تشخیصی نیست.
هر یک از این نمونهها نشان میدهند که چگونه نقشهی sensor مستقیماً تفسیر بالینی را هدایت کرده است: موقعیت قلهی ریتم روی پوست سر، فرضیههای بالینی را شکل داده است.
یکی از نوآوریهای سیستم گزارشدهی QEEGhome، پنل اختصاصی sensor-based localization است که منشأ فضایی هر یک از باندهای اصلی فرکانسی EEG را به شکل شهودی و قابل درک به تصویر میکشد.
در این سیستم، برخلاف روشهایی که تنها جدولهایی از z-score ها یا شاخصهای کلی ارائه میدهند، گزارش شامل نقشههای توپولوژیک از سر برای باندهای delta، theta، alpha، beta، high beta(و در صورت ارزیابی، gamma) است که در آنها محل دقیق الکترودهایی که بیشترین فعالیت را در هر باند نشان میدهند به وضوح مشخص شدهاند.
دلتا (۱ تا ۳ هرتز): در بزرگسالان بیدار معمولاً پاتولوژیک است، مثلاً در آسیب مغزی یا انسفالوپاتی دیده میشود.
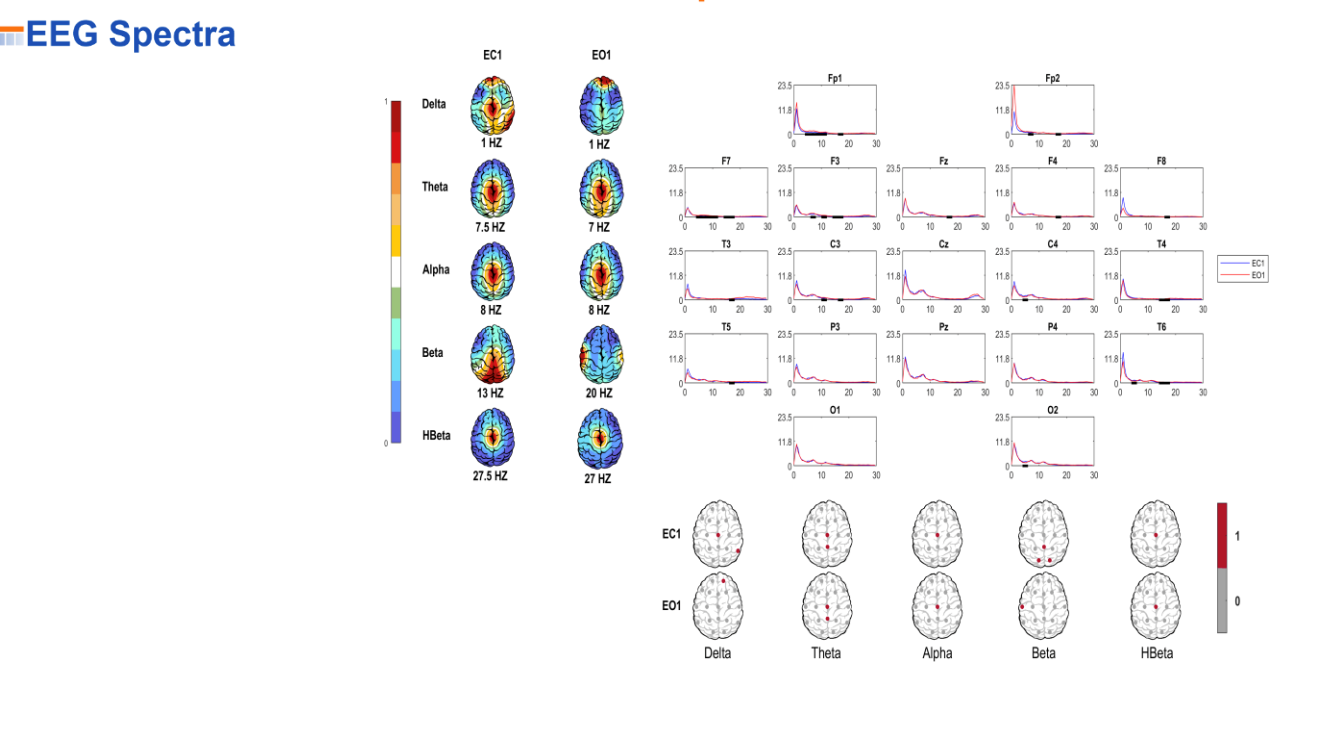
در گزارش QEEGhome، هر باند فرکانسی (Delta، Theta، Alpha، Beta، High-Beta) به صورت نقشهای رنگی از پوست سر (Scalp Map) نشان داده میشود، و نقاط قرمز محل الکترودهایی را نشان میدهند که بیشترین توان (Power) در آن باند خاص را دارند.
در مثال یک فرد سالم، باند Alpha بیشترین فعالیت را در نواحی posterior دارد که نشان دهندهی الگوی نرمال posterior dominant alpha است، در حالی که Beta در ناحیهی Fronto-Central متمرکز شده که الگوی طبیعی برای هوشیاری است.
همان طور که در تصویر بالا نمایش داده شده،QEEGhome دادههای هر باند را در قالب نقشهای ساده و قابل تفسیر ارائه میدهد. در هر نقشه، رنگها توزیع توان را نمایش میدهند (رنگهای گرم = توان بیشتر، رنگهای سرد = توان کمتر) و یک نقطهی قرمز دقیقاً روی الکترودی که بیشترین مقدار را در آن باند دارد قرار میگیرد یا اگر اشتباهی در localization رخ دهد، ممکن است منبع اشتباهی هم مشخص شود.
این کار به پزشک اجازه میدهد تا تنها با یک نگاه به سوالاتی از این دست پاسخ دهد:
آیا آلفای بیمار از occipital میآید؟
فعالیت سریع Beta دقیقاً کجای سر متمرکز شده؟
گزارش اغلب مقایسههای Side-by-Side نیز ارائه میدهد مثلاً حالت چشم باز در مقابل چشم بسته تا مشخص شود که منشأ هر ریتم با تغییر وضعیت چگونه تغییر میکند.
برای مثال، در ضبط چشم بستهی طبیعی، انتظار میرود نقطهی آلفا روی O1/O2 ناحیه occipital قرار بگیرد و نقاط Beta روی Fz یا Cz ناحیه Frontal/Central قرار داشته باشند.
اگر این الگوهای مورد انتظار رعایت شده باشند، الگوی فضایی طبیعی است. در غیر این صورت، بلافاصله ناحیهای برای بررسی بالینی مشخص میشود.
برای نمونه:
اگر نقطهی آلفا روی ناحیهی Frontal و نه Occipital باشد، احتمال "Frontal Alpha" مطرح میشود که میتواند نشان دهندهی افسردگی باشد.
اگر نقشهی Beta در نواحی Posterior روشن باشد و نقطه روی Pz یا O2 باشد، این یک localization غیر عادی است که ممکن است مربوط به اضطراب، برانگیختگی بیش از حد Hyperarousal یا حتی آرتیفکت باشد.
نکتهی کلیدی این است که پزشک نیاز به جست و جوی خسته کننده در میان صفحات اعداد ندارد؛ گزارش با یک نگاه، مشاهدات بالینی مهم را نمایان میسازد.
با پیاده سازی این روش، QEEGhome در واقع تحلیل کمی را با رویکرد الگو محورِ تفسیر EEG سنتی ترکیب میکند.
این رویکرد به پزشک اجازه میدهد تا دانش نوروفیزیولوژی خود را مستقیماً به کار ببرد: نقشهی هر باند فرکانسی با آنچه دربارهی محل طبیعی یا غیر طبیعی آن میدانیم مقایسه میشود.
این کار باعث میشود که کاربرد بالینی QEEG به طور چشمگیری افزایش یابد.
پزشک به جای غرق شدن در دهها شاخص اتوماتیک، با یک نقشهی فرکانسی روشن از مغز مواجه میشود.
از آنجا به بعد، کار تفسیر به تشخیص الگوها تبدیل میشود:
آیا الگوی فعالیت طبیعی است؟
آیا قلههای غیر منتظرهای وجود دارد؟
کدام ناحیهها از حالت نرمال انحراف دارند؟
این تمرکز بر الگوها و منبع فعالیت تضمین میکند که هرگونه مداخله (از نوروفیدبک گرفته تا دارو درمانی یا ارجاع برای ارزیابیهای بیشتر) بر پایهی دینامیک واقعی مغز بیمار انجام شود.
روش Sensor-Based Source Localization در QEEG تفسیر را شفاف و بر اساس اصول پایهی نوروفیزیولوژی EEG قرار میدهد.
با تمرکز بر توپوگرافی سطحی هر باند فرکانسی، پزشکان فوراً میتوانند تشخیص دهند که آیا ریتمهای مغزی در محل طبیعی خود قرار دارند (مانند آلفای occipital، بتای frontal) یا دچار جا به جایی شدهاند.
این رویکرد بسیاری از اشتباهات Inverse Modeling و تکیهی بیش از حد بر مقایسههای z-score را دور میزند و نتایج کمی را با دههها پژوهش EEG پیوند میدهد.
در عمل، یافتن نقاط داغ Hotspots برای آلفا یا بتا روی نقشهی سنسوری اغلب با تشخیصهای بالینی خاص هم راستا بوده و مسیر ارزیابی را مشخص میکند.
در حالیکه تصویر برداریهای پیشرفتهی منبع جایگاه خود را در تحقیقات دارند، در گزارشهای روتین QEEG بیشترین فایده زمانی حاصل میشود که تأکید روی این باشد که هر ریتم کجا روی سر بیشترین قدرت را دارد.
این باعث میشود که تحلیلهای پیشرفته نیز هم چنان در واقعیت قابل مشاهدهی EEG ریشه داشته باشند و بینشهای عملی برای مراقبت از بیمار فراهم کنند.
Britton, J. W., Frey, L. C., & Hopp, J. L. et al. (2016). Electroencephalography (EEG): An Introductory Text and Atlas of Normal and Abnormal Findings in Adults, Children, and Infants. American Epilepsy Society.
Nuwer, M. R., Buchhalter, J., & Shepard, K. M. (2016). Quantitative EEG in attention-deficit/hyperactivity disorder: A companion payment policy review for clinicians and payers. Neurology: Clinical Practice, 6(6), 543–548.
Ribas, V. R., Ribas, R. G., Nóbrega, J. A., Ferracioli-Oda, E., Ribeiro, I., & Martins, H. A. (2018). Pattern of anxiety, insecurity, fear, panic and/or phobia observed by QEEG. Dementia & Neuropsychologia, 12(3), 264–271.
Ji, Y., Choi, T. Y., Lee, J., Yoon, S., Won, G. H., Jeong, H., Kang, S. W., & Kim, J. W. (2022). Characteristics of attention-deficit/hyperactivity disorder subtypes in children classified using quantitative EEG. Neuropsychiatric Disease and Treatment, 18, 2725–2736.
Luo, Y., Tang, M., & Fan, X. (2025). Meta analysis of resting frontal alpha asymmetry as a biomarker of depression. NPJ Mental Health Research, 4, 2.
Garcés, P., Vicente, R., Wibral, M., Pineda-Pardo, J. Á., López, M. E., Aurtenetxe, S., et al. (2013). Brain-wide slowing of spontaneous alpha rhythms in mild cognitive impairment. Frontiers in Aging Neuroscience, 6, 77.