
انتخاب داروی مناسب در روانپزشکی، یکی از چالش برانگیزترین تصمیمات است. برخلاف بسیاری از شاخههای پزشکی که در آنها ابزارهایی نظیر آزمایشهای خونی، تصویربرداری پیشرفته یا پنلهای ژنتیکی در انتخاب درمان نقش تعیینکننده دارند، تصمیمگیری دارویی در روانپزشکی تا مدتها به رویکرد «آزمون و خطا» متکی بوده است. این رویکرد سنتی، گرچه در برخی موارد کارآمد است، اما اغلب با پیامدهایی مانند تأخیر در شروع پاسخ درمانی، بروز عوارض جانبی، استفاده همزمان از چند دارو (پلیفارماسی) و مهمتر از همه، رنج طولانی مدت بیمار، همراه است. چنین وضعیتی، نیاز مبرمی به ابزارهایی دقیق، فردمحور و قابل اعتماد برای انتخاب دارو را آشکار میکند.
در نتایج یکی از بزرگترین و جامعترین مطالعات بالینی در درمان افسردگی، محدودیتهای رویکرد آزمون و خطا بهروشنی قابل مشاهده است. این مطالعه نشان داد که تنها حدود ۳۰٪ از بیماران در همان مرحله اول و با دریافت نخستین داروی ضدافسردگی به بهبودی کامل دست مییابند. در صورت عدم پاسخ اولیه، با هر مرحله درمانی بعدی، احتمال موفقیت کاهش یافته است. در نهایت، نزدیک به ۷۰٪ از بیماران برای یافتن یک داروی مؤثر ناچار به طی کردن چندین دوره درمانی بودند، فرآیندی که در بسیاری از موارد ماهها یا حتی سالها به طول انجامیده است [1].
در بسیاری از حوزههای پزشکی، استفاده از نشانگرهای زیستی (Biomarkers) در فرآیند درمان، موجب افزایش چشمگیر اثربخشی مداخلات بالینی شده است. در رشتههایی نظیر سرطانشناسی، بیماریهای قلبی-عروقی و عفونی، این نشانگرها نقش کلیدی در انتخاب دارو، تعیین شدت بیماری، و پیشبینی پاسخ به درمان ایفا میکنند. در سالهای اخیر، روانپزشکی نیز بهسوی بهرهگیری از چنین رویکردهای دادهمحور حرکت کرده است، رویکردی که زمینهساز گذار از درمانهای یکسان برای همه، به سمت درمانهای فردمحور و مبتنی بر ویژگیهای زیستی هر بیمار است.
در روانپزشکی، به نشانگرهای objective مبتنی بر فعالیت مغزی، نشانگرهای عصبی (Neuromarkers) گفته میشود. در میان ابزارهای مختلف نوروفیزیولوژیک و تصویربرداری مانند تصویربرداری PET ، fMRI و DTI، نورومارکرهای مبتنی بر الکتروانسفالوگرافی (Electroencephalography - EEG) به یکی از کاربردیترین ابزارها برای استفاده بالینی تبدیل شدهاند. EEG روشی غیرتهاجمی، مقرونبهصرفه و در دسترس است که اطلاعات عملکردی بلادرنگ (real-time) درباره دینامیک فعالیت مغز ارائه میدهد. شکل توسعهیافتهی این روش، یعنی الکتروانسفالوگرافی کمی(Quantitative EEG - QEEG) ، با تبدیل سیگنالهای خام EEG به الگوهای عددی، امکان مقایسه objective این دادهها میان افراد و گروههای مختلف را فراهم میسازد. بدینترتیب، QEEG زمینهای فراهم میکند تا مغز، نهتنها بهعنوان یک اندام شناختی، بلکه بهعنوان یک ابزار کمک تشخیصی و پیشبینیکننده بالینی مورد استفاده قرار گیرد.

در دو دهه گذشته، پژوهشهای متعددی منجر به شناسایی نورومارکرهای مبتنی بر EEG شدهاست که میتوانند بهعنوان پیشبینیکنندههای پاسخ به درمان دارویی در اختلالات روانپزشکی عمل کنند.
این نورومارکرها شامل شاخصهای مختلفی هستند، از جمله:
توان طیفی (Spectral Power) ،
ناتقارنی امواج (Asymmetry) ،
مکانیابی سیگنالها (Source-Localized Activity) ،
و معیارهای مبتنی بر شبکههای دینامیک مغزی (Dynamic Brain Network Metrics) [2].
این نورومارکرها نوید آن را میدهند که در آیندهای نزدیک، انتخاب درمان دارویی بتواند به جای آزمون و خطا، بر پایهی دادههای قابل سنجش و اختصاصی از عملکرد مغز هر فرد صورت گیرد.
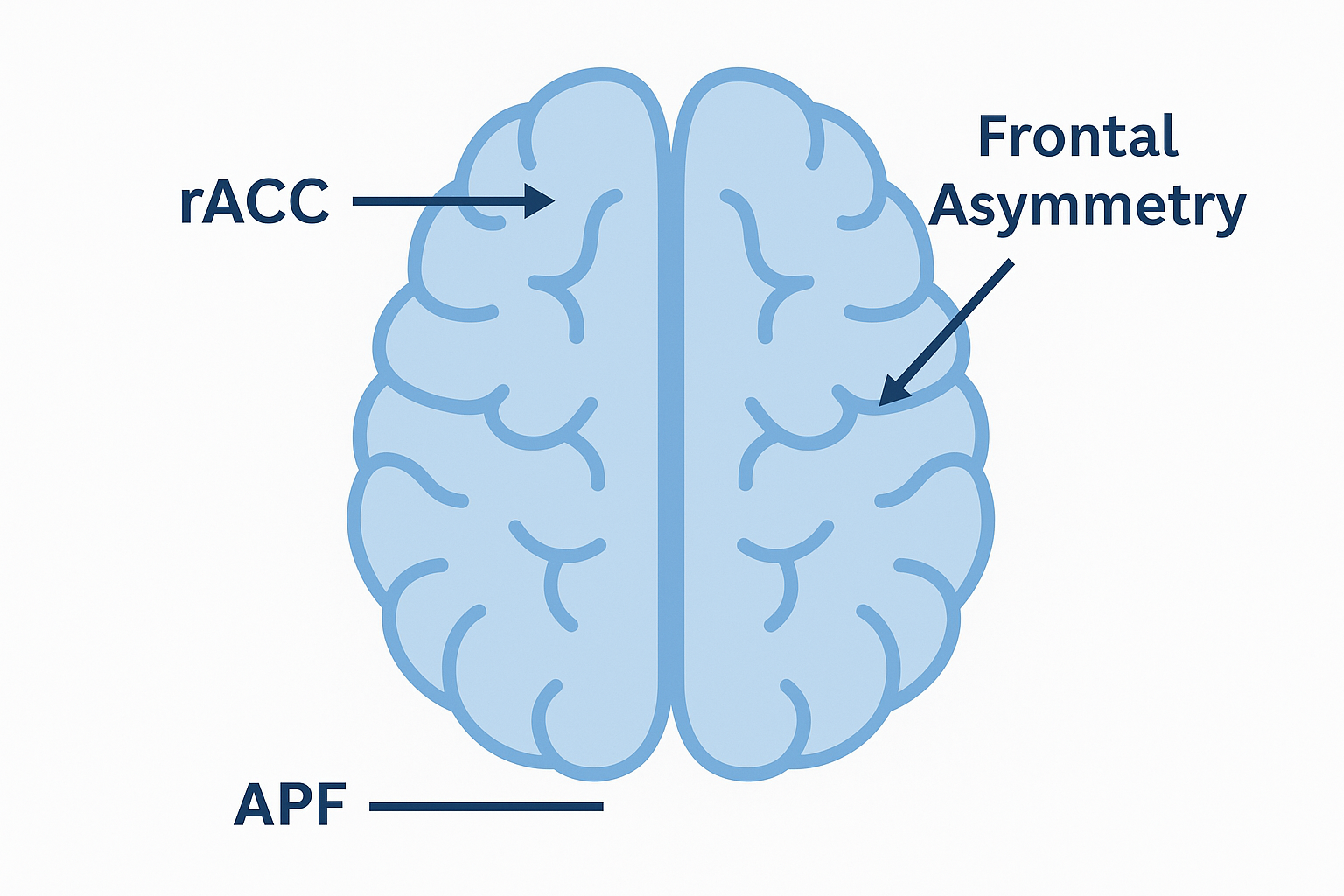
- فعالیت تتا در ناحیه سینگولیت قدامی راست (rACC) بهعنوان پیشبینیکننده پاسخ به داروهای ضدافسردگی: افزایش فعالیت باند تتا در قشر سینگولیت قدامی راست (Right Anterior Cingulate Cortex - rACC) یکی از پایدارترین و معتبرترین نورومارکرهای مبتنی بر EEG در پیشبینی پاسخ به درمانهای ضدافسردگی محسوب میشود. مطالعات متعدد نشان دادهاند که افزایش توان تتا در این ناحیه با احتمال بالاتر پاسخگویی به داروهای مهارکننده بازجذب سروتونین (Selective Serotonin Reuptake Inhibitors - SSRIs) و داروهای مهارکننده بازجذب سروتونین-نوراپینفرین (Serotonin–Norepinephrine Reuptake Inhibitors - SNRIs) همبستگی دارد. شواهد پژوهشی گزارش کردهاند که این نشانگر میتواند در برخی زیرگروههای بیماران مبتلا به افسردگی، احتمال پاسخ به دارو را با دقتی حدود ۷۴٪ پیشبینی کند [3].
- عدم تقارن آلفای پیشانی بهعنوان نشانگر پاسخ به درمان در افسردگی: یکی دیگر از نورومارکرهای شناختهشده در پیشبینی پاسخ به درمان در افسردگی، الگوی عدم تقارن امواج آلفا در نواحی پیشانی (Frontal Alpha Asymmetry) است. در این الگو، افزایش توان آلفا در نیمکره راست پیشانی نسبت به چپ که نشاندهنده فعالیت نسبی کمتر قشر پیشانی چپ است، با پاسخ مثبت به داروهای مهارکننده بازجذب سروتونین (SSRIs) در بیماران زن ارتباط دارد. این نشانگر همچنین با فعالسازی سیستمهای انگیزشی مغز که در پاتوفیزیولوژی افسردگی نقش دارند، مرتبط دانسته شده است. به همین دلیل، میتواند در تمایز بین پاسخ به کلاسهای مختلف داروهای ضدافسردگی مفید واقع شود [4].
- کاهش کوردنس تتای پیشانی بهعنوان نشانگر اولیه پاسخ درمانی: شاخص کوردنس تتا در ناحیه پیشانی (Frontal Theta Concordance) یکی از معیارهای تحلیلی در QEEG است که با ادغام توان مطلق و نسبی در باند تتا، تصویر دقیقتری از فعالیت نواحی پیشانی ارائه میدهد. مطالعات نشان دادهاند که کاهش کوردنس تتا در نواحی پیشانی در طول هفته اول پس از شروع داروی ضدافسردگی، حتی پیش از بروز علائم بالینی آشکار، میتواند پیشبینیکننده قابل اعتمادی برای پاسخدهی به درمان باشد [5]. این ویژگی، QEEG را به ابزاری مؤثر در پایش زودهنگام اثربخشی درمان تبدیل میکند.
- فرکانس APF و ارتباط آن با پاسخ شناختی و درمانی: فرکانس (Alpha Peak Frequency - APF) یکی از شاخصهای مهم در تحلیل QEEG است که نشاندهنده سطح برانگیختگی و همزمانی (Synchrony) در قشر مغز میباشد. مطالعات نشان دادهاند که کاهش APF با کندی در پردازش شناختی و نیز با پاسخ ضعیف به داروهای ضدافسردگی سنتی نظیر SSRIs ارتباط دارد. در مقابل، افزایش یا نزدیک شدن APF به محدوده بهینه، در طول درمان با بهبود علائم افسردگی همبستگی مثبتی نشان داده است [6]. این ویژگی، APF را به یکی از نورومارکرهای بالقوه در پایش پیشرفت درمان و انتخاب نوع مداخله دارویی تبدیل میکند.
- نسبت تتا به بتا در ADHD بهعنوان نورومارکر پاسخ به داروهای محرک: نسبت تتا به بتا (Theta/Beta Ratio - TBR) یکی از نورومارکرهای شناختهشده و مورد مطالعه در اختلال ADHD است. مقادیر بالای TBR در کودکان و نوجوانان مبتلا به ADHD معمولا با سطوح بالاتر بیتوجهی، بیشفعالی و کاهش عملکرد اجرایی قشر پیشپیشانی (Prefrontal Cortex) همراه است. این نشانگر، نهتنها ارزش کمک تشخیصی دارد، بلکه بهعنوان پیشبینیکننده پاسخ به داروهای محرک از جمله متیلفنیدیت (Methylphenidate) نیز مورد توجه قرار گرفته است. پژوهشها نشان دادهاند که پاسخدهندگان به متیلفنیدیت، در طول درمان معمولا روند تدریجی بازگشت نسبت تتا/بتا به الگوی طبیعی را نشان میدهند، یعنی کاهش نسبت غیرطبیعی تتا به بتا به سمت مقادیر مشاهدهشده در افراد سالم [7].
نورومارکرها نهتنها در پیشبینی احتمال اثربخشی یک دارو نقش دارند، بلکه میتوانند دربارهی مدت زمان لازم برای بروز پاسخ درمانی و همچنین ضرورت احتمالی بهکارگیری داروهای تقویتی یا ترکیبی، بینشهای بالینی ارزشمندی ارائه دهند.

متاآنالیزها و مطالعات بالینی اخیر نشان دادهاند که بهرهگیری نورومارکرهای مبتنی بر EEG در فرآیند انتخاب داروهای ضدافسردگی، میتواند میزان پاسخ درمانی را نسبت به تجویزهای سنتی مبتنی بر صرف علائم بالینی، بین ۲۵ تا ۵۰ درصد افزایش دهد [5]. این یافتهها نشان میدهند که ادغام دادههای نوروفیزیولوژیک در تصمیمگیری درمانی نهتنها امکان شخصیسازی مداخله را فراهم میسازد، بلکه میتواند اثربخشی درمان را بهطور معناداری بهبود بخشد.
بر پایه نتایج مطالعات بالینی:
در بیمارانی که تجویز داروی ضدافسردگی بر اساس پروفایل EEG انجام شده بود، نرخ کلی بهبودی از حدود ۳۰٪ به بیش از ۵۰٪ افزایش یافت.
میانگین زمان دستیابی به پاسخ بالینی معنادار در این بیماران، بین ۲ تا ۴ هفته کوتاهتر از گروههای دریافتکننده درمان سنتی بود.
تعداد تجویزهای ناموفق (آزمونهای دارویی بیاثر) نیز بهطور چشمگیری کاهش یافت.
این پیشرفتها نهتنها از نظر بالینی قابل توجه هستند، بلکه میتوانند با کاهش هزینههای مراقبت سلامت، کاهش رنج بیمار و پیشگیری از مزمن شدن یا مقاوم شدن اختلال به درمان، تأثیرات اقتصادی و انسانی گستردهای داشته باشند.
در حالیکه بسیاری از سامانههای مرسوم الکتروانسفالوگرافی کمی همچنان به مقایسههای محدود بر اساس ویژگیهای z-score و نقشههای توپوگرافی فرکانسی متکی هستند، پلتفرم QEEGhome رویکردی نوین و منطبق با نیازهای بالینی روانپزشکی ارائه میدهد. گزارشهای نقشه مغزی تولیدشده توسطQEEGhome ، فراتر از تحلیل توان باندهای فرکانسی، شامل عناصر پیشرفته زیر هستند:
تفسیرهای مبتنی بر تشخیص بالینی، با اتکا به پایگاههای داده ترکیبی از جمعیت نرمال و بیماران پاتولوژیک؛
جداول پیشبینی پاسخ دارویی با استفاده از الگوریتمهای یادگیری ماشین(Machine Learning) ، که بر پایهی تلفیق چندین دهه از یافتههای تحقیقاتی در حوزه EEG و درمانهای دارویی طراحی شدهاند؛
نورومارکرهای شخصیسازیشده با خروجی گرافیکی مناسب، که به سهولت تفسیر پزشک کمک میکند.
نمودار پیشبینی پاسخ دارویی پلتفرم QEEGhome بر پایه بیش از ۴۷۰ سابجکت و ۸۵ نورومارکر طراحی شده است. این مدل با ادغام نتایج مطالعات معتبر منتشرشده از سال ۱۹۷۰ تا ۲۰۲۱، مجموعهای غنی از دادههای تجربی را در قالب یک ابزار کاربردی بالینی در اختیار متخصصان قرار میدهد.
نورومارکرهای استفادهشده در این مدل شامل:
الگوهای اتصال پویا (Dynamic Connectivity Patterns) ،
ویژگیهای غیرخطی (Nonlinear Features) ،
و شاخصهای Bispectral میباشند.
در نتیجه، نمودار ارائهشده توسط QEEGhome بهعنوان یک مدل پیشبینی قابل استفاده در تصمیمگیری بالینی، امکان پیشبینی پاسخ درمانی در گروههای مختلف دارویی را بهصورت شخصیسازیشده فراهم میسازد.
نورومارکرهای مبتنی بر EEG نویدبخش آغاز عصر جدیدی در روانپزشکی هستند، عصری که در آن، عملکرد مغز مبنای تصمیمگیریهای درمانی قرار میگیرد. در پلتفرم QEEGhome، تلاش کردهایم تا شکاف میان پژوهشهای پیشرفته و عمل بالینی روزمره را از میان برداریم. این سامانه، با بهرهگیری از دادههای کمّی قابل تفسیر، به روانپزشکان این امکان را میدهد که انتخاب دارو بر پایه اطلاعات نوروفیزیولوژیکی دقیق و متناسب با هر فرد داشته باشند. گزارشهای پلتفرم QEEGhome بهگونهای طراحی شدهاند که پزشک را از تفسیر پیچیده سیگنالهای خام یا نقشههای توپوگرافیک بینیاز میکنند. در عوض، دادههایی بصری، مبتنی بر شواهد علمی و پیشبینیگر ارائه میدهند که از تصمیمگیری بالینی مؤثر، بهموقع و متناسب با نیاز هر بیمار پشتیبانی میکنند.
آینده روانپزشکی، صرفا در مصاحبه بالینی با بیمار خلاصه نمیشود؛ بلکه در توانایی ما برای «شنیدن صدای مغز» نهفته است و این چشمانداز، با بهرهگیری ازQEEG ، به واقعیت بالینی تبدیل میشود.
1. Trivedi, M. H., et al. (2006). Evaluation of outcomes with citalopram for depression using measurement-based care in STARD: implications for clinical practice. American Journal of Psychiatry, 163(1), 28–40.
2. Johnstone, S. J., Barry, R. J., & Clarke, A. R. (2013). Ten years on: A follow-up review of ERP research in attention-deficit/hyperactivity disorder. Clinical Neurophysiology, 124(4), 644–657.
3. Pizzagalli, D. A., Webb, C. A., et al. (2018). Pretreatment rostral anterior cingulate cortex theta activity in relation to symptom improvement in depression: a randomized clinical trial. JAMA Psychiatry, 75(6), 547–554.
4. Arns, M., Bruder, G., et al. (2015). EEG alpha asymmetry as a gender-specific predictor of treatment response to antidepressants in major depressive disorder. European Neuropsychopharmacology, 25(5), 823–831.
5. Cook, I. A., et al. (2002). Early changes in prefrontal activity characterize clinical responders to antidepressants. Neuropsychopharmacology, 27(1), 120–131.
6. Kemp, A. H., Gordon, E., Rush, A. J., Williams, L. M. (2008). EEG alpha asymmetry in major depressive disorder and its association with therapeutic response to selective serotonin reuptake inhibitors. Biological Psychology, 77(2), 289–292.
7. Arns, M., Conners, C. K., & Kraemer, H. C. (2013). A decade of EEG Theta/Beta ratio research in ADHD: a meta-analysis. Journal of Attention Disorders, 17(5), 374–383.